Sarcomul Ewing
Toate informațiile oferite aici sunt doar de natură generală, terapia tumorală aparține întotdeauna în mâinile unui oncolog cu experiență!
Sinonime
Sarcom osos, PNET (tumoră neuroectodermică primitivă), tumoră Askin, Ewing - sarcom osos
Engleză: sarcomul lui Ewing
definiție
In care Sarcomul Ewing este un de la Măduvă osoasă de ieșire Tumora osoasăcare poate apărea între 10 și 30 de ani. Cu toate acestea, afectează mai ales copiii și tinerii până la vârsta de 15 ani. Sarcomul lui Ewing este mai puțin obișnuit osteosarcom.
Sarcomul lui Ewing este localizat în cele lungi Oase lungi (Femur (Osul coapsei) și tibia (Shin)), precum și în pelvis sau coaste. În principiu, cu toate acestea, toate oasele trunchiului și ale scheletului membrelor pot fi afectate, metastaza în special în plămânii este posibil.
frecvență
Probabilitatea de a dezvolta sarcoame Ewing este <1: 1.000.000. Studiile au arătat că pentru fiecare milion de oameni care trăiesc acolo, aproximativ 0,6 pacienți noi dezvoltă sarcoame Ewing în fiecare an.
Comparativ cu osteosarcomul (aproximativ 11%) și condrosarcomul (aproximativ 6%), sarcomul Ewing se află pe locul al treilea ca un alt reprezentant al tumorilor osoase primare maligne. În timp ce sarcomul lui Ewing apare mai ales între 10 și 30 de ani, o manifestare principală ar putea fi stabilită în a doua decadă a vieții (15 ani). Prin urmare, se manifestă mai ales în scheletul în creștere, băieții (56%) suferind de sarcom Ewing puțin mai des decât fetele. Dacă comparați tumorile osoase primare maligne ale copiilor și adolescenților, sarcomul Ewing este pe locul doi: La sarcoamele osoase ale copiilor, proporția așa-numitelor osteosarcoame este de aproximativ 60%, proporția sarcoamelor Ewing în jur de 25% .
cauze
Așa cum a fost deja explicat și prezentat în contextul rezumatului, cauza care este responsabilă pentru dezvoltarea Sarcomul Ewing nu poate fi lămurit pe deplin. S-a constatat însă că sarcoamele Ewing apar adesea atunci când există anomalii scheletice familiale sau pacienți sub unul de la naștere retinoblastom (= tumoră retiniană malignă care apare la adolescență). Cercetările au arătat că celulele tumorale din așa-numita familie de sarcoame Ewing au o schimbare Cromosomul # 22 expoziţie. Se crede că această mutație este prezentă la aproximativ 95% din toți pacienții.
localizare
Cele mai frecvente locații ale sarcomului Ewing pot fi găsite în oasele tubulare lungi, în special în tibia și fibula sau în oasele plate. Cu toate acestea, ca cancer osos malign, sarcomul Ewing poate afecta toate oasele. Oasele mai mari sunt afectate cel mai frecvent, cele mai mici rareori. Dacă oasele tubulare lungi sunt afectate, tumora se găsește de obicei în zona așa-numitei diafize, zona axului.
Locații preferate:
- aproximativ30% femur (osul coapsei)
- aproximativ 12% tibie (shin)
- aproximativ 10% humerus (osul brațului superior)
- aproximativ 9% bazin
- aproximativ 8% fibula (fibula).
Din cauza metastazelor hematogene severe care apar mai devreme (vezi secțiunea următoare), este posibilă localizarea țesuturilor moi.
Localizare în pelvis
Sarcomul Ewing este localizat în osul pelvin ca fiind tumora primară (locul de origine al tumorii) în doar aproximativ al cincilea caz. Mult mai des, însă, tumora primară este localizată într-un os tubular lung.
Primele simptome pot fi umflarea, durerea și supraîncălzirea în zona pelvină.
Localizare în picior
Piciorul este o localizare rară într-o tumoră primară. Este mai frecvent ca tumorile primare din tibie sau fibulă să favorizeze o metastază la nivelul piciorului.
Dacă există umflarea dureroasă neclară și supraîncălzirea piciorului, în special în adolescență, sarcomul Ewing ar trebui, de asemenea, să fie exclus în plus față de artrita juvenilă. Cel mai rău nu trebuie neapărat asumat aici. Diagnosticările direcționate sub formă de imagistică pot oferi claritate inițială despre cauzele reclamațiilor.
metastază
După cum am menționat mai sus, acest lucru se aplică Sarcomul lui Ewing ca metastază hematogenă precoce (= prin fluxul sanguin). Prin urmare, metastazele se pot instala și în țesutul moale. Dintre acestea, în primul rând este plămân afectat. Cu toate acestea, scheletul poate fi afectat și de metastaze prin fluxul sanguin.
Faptul că sarcomul Ewing trebuie clasificat ca metastatic timpuriu este demonstrat de studii care arată că metastazele pot fi detectate în aproximativ 25% din toate cazurile în momentul diagnosticării. Din moment ce, din păcate, metastazele nu pot fi întotdeauna descoperite, rata de întuneric este probabil mult mai mare.
diagnostic
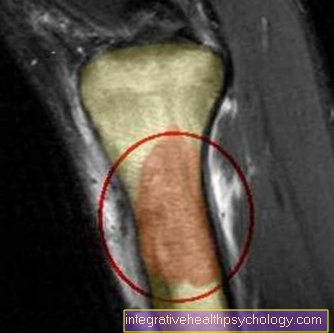
Sarcoamele Ewing pot provoca o varietate de simptome. Acestea ar trebui să fie enumerate mai jos:
- Durere de cauză necunoscută
- Umflarea și durerea de obicei în regiunea / regiunile afectate
- Umflarea ganglionilor limfatici
- semne locale de inflamație (înroșire, umflare, supraîncălzire)
- pierderea în greutate nedorită
- Restricții funcționale până la paralizie
- Fractură fără un accident
- Transpirații de noapte
- leucocitoză moderată (= creșterea numărului de leucocite în sânge)
- scăderea performanței
O tumoare poate fi exclusă cu o probabilitate suficientă dacă următoarele criterii sunt îndeplinite în conformitate cu diagnosticul clinic, imagistică și de laborator:
- Nu există nicio dovadă a unei mase
sau
Umflarea vizibilă, masa dovedită sau plângerile neclare pot fi clar explicate și documentate printr-o boală non-tumorală.
Diagnostic de bază:
În principiu, metodele de imagistică sunt utilizate pentru diagnosticarea de bază. acestea sunt
Examinarea radiografiei
Examinarea radiografiei în zona localizării tumorii (cel puțin 2 niveluri)
ecografie
Sonografia tumorii (mai ales dacă este suspectată o tumoare cu țesut moale în diagnosticul diferențial)
Pentru a obține informații suplimentare și pentru a permite delimitarea diagnosticului diferențial, se utilizează diagnostice de laborator (examinarea valorilor de laborator). Următoarele valori sunt determinate ca parte a acestei diagnosticări de laborator:
- Hemoleucograma
- Fier (deoarece scade în tumori)
- Electroliți (pentru a exclude hipercalcemia)
- ESR (rata de sedimentare)
- CRP (proteină C-reactivă)
- fosfatază alcalină (aP)
- specifice osului (AP)
- Fosfataza acidă (sP)
- Antigen specific de prostată (PSA)
- Acidul uric (HRS): crescut odată cu cifra de afaceri ridicată a celulelor, de ex. în hemoblastoză
- Proteine totale: scădere în procesele consumatoare
Electroforeză proteică - Starea urinei: paraproteine - dovezi ale mielomului (plasmacitom)
- Markerul tumoral NSE = enolază specifică neuronului în sarcomul Ewing
Diagnostic tumoral special
Imagistica prin rezonanta magnetica (RMN)
În plus față de metodele imagistice menționate în contextul diagnosticului de bază, tomografia prin rezonanță magnetică reprezintă o posibilitate suplimentară care poate fi utilizată în cazuri individuale.
Folosind RMN (tomografie prin rezonanță magnetică), țesutul moale poate fi arătat deosebit de bine, prin care poate fi arătată expansiunea tumorii către structurile vecine (nervi, vase) ale oaselor afectate. Mai mult, volumul tumorii poate fi estimat folosind RMN (tomografie prin rezonanță magnetică) și amploarea locală a tumorii poate fi clarificată.
De îndată ce se suspectează o tumoră osoasă malignă, ar trebui să se imagineze că întregul os purtător de tumoră exclude metastaze (așezări maligne).
Tomografie computerizată (CT):
(în special pentru a arăta structuri osoase dure (corticale))
Tomografie cu emisie de pozitroni (PET)
(Valoarea nu este încă suficient de valabilă)
Citiți mai multe despre acest subiect: Tomografie cu emisie de pozitroni
Angiografia cu scădere digitală (DSA) sau angiografia pentru vizualizarea vaselor tumorale
Scintigrafie scheletică (scintigrafie în 3 faze)
biopsie
Așa cum am menționat de mai multe ori, diferența dintre sarcomul Ewing și osteomielita, de exemplu, poate fi destul de dificilă. Pe lângă faptul că simptomele sunt similare, radiografia ca atare nu poate oferi întotdeauna informații directe. Dacă, după așa-numitele diagnostic neinvazive descrise mai sus, există încă suspiciunea unei tumori sau dacă există o incertitudine cu privire la tipul și demnitatea unei tumori, ar trebui efectuat un examen histopatologic (= examinare tisulară).
Proceduri deschise
Biopsia incizională
Ca parte a așa-numitei biopsii incizionale, tumora este expusă parțial chirurgical. În cele din urmă, se prelevează o probă de țesut (dacă este posibil țesut osos și moale) Țesutul tumoral eliminat poate fi evaluat direct.
Biopsie excițională (îndepărtarea completă a tumorii)
Se consideră numai în cazuri excepționale, de exemplu, dacă există suspiciunea de malignitate (trecerea de la tumora benignă la cea malignă) a osteocondromelor mai mici.
terapie
Abordarea terapeutică aici este de obicei pe mai multe niveluri. Pe de o parte, așa-numitul plan de terapie prevede de obicei un tratament chimioterapeutic preoperator (= chimioterapie neoadjuvantă). Chiar și după îndepărtarea chirurgicală a sarcomului Ewing, tratamentul terapeutic de urmărire este asigurat prin radioterapie și, dacă este necesar, chimioterapie reînnoită. Aici se observă o diferență de osteosarcom: în comparație cu sarcomul Ewing, osteosarcomul are o sensibilitate mai mică la radiații.
Obiectivele terapiei:
O așa-numită abordare terapeutică curativă (vindecătoare) este dată în special la pacienții al căror sarcom Ewing este localizat și nu prezintă metastaze. Între timp, așa-numita chimioterapie neoadjuvantă în combinație cu chirurgia și radioterapia deschide oportunități suplimentare. Dacă sarcomul Ewing metastazează în afara plămânilor (= boală tumorală generalizată; metastaze extrapulmonare), terapia are de obicei un caracter paliativ (care se prelungește viața) (vezi mai jos).
Modalități de terapie:
local:
- chimioterapie preoperatorie
- terapie chirurgicală (rezecție largă sau radicală după Enneking)
- radioterapie
sistemică:
chimioterapie antineoplastică
- Terapia combinată (în primul rând (= "prima linie"): doxorubicină, ifosfamidă, Metotrexatul / Leukovorină, cisplatină; în a doua linie (= "a doua linie"): etoposid și carboplatină)
(Protocoalele se pot schimba la scurt timp)
Terapia curativă:
- chimioterapie agresivă cu mai multe substanțe pre și postoperator
- Tratament local sub formă de rezecție tumorală chirurgicală sau radiație singură
- Suplimentează terapia cu Pre-iradiere (de exemplu, în cazul tumorilor nefuncționale, care nu răspund) sau prin post-iradiere
- Este important de menționat în contextul terapiei chirurgicale că, în special din cauza dezvoltării ulterioare a metodelor chirurgicale, sunt posibile intervenții care păstrează extremitățile în multe cazuri. Cu toate acestea, perspectiva unei cure are întotdeauna prioritate, astfel încât accentul ar trebui să fie întotdeauna pus pe radicalitate (= calitate oncologică) și nu pe posibila pierdere a funcției.
- Chimioterapia poate fi continuată (vezi mai sus). Se vorbește apoi despre o așa-numită consolidare.
- La pacienții cu metastaze pulmonare, pot fi necesare intervenții suplimentare în zona plămânilor, cum ar fi îndepărtarea parțială a plămânilor.
Terapie paliativă (care prelungește viața):
Pacienții care au o boală tumorală generalizată (= metastaze extrapulmonare) trebuie să localizeze tumora primară pe trunchi și / sau tumora primară se dovedește a fi inoperabilă. În astfel de cazuri, este posibilă numai terapia paliativă. În astfel de cazuri, accentul se concentrează, de obicei, pe menținerea calității vieții, astfel încât terapia se concentrează pe ameliorarea durerii și menținerea funcției.
prognoză
Dacă apar sau nu recurențe depinde puternic de amploarea metastazelor, de răspunsul la chimioterapia preoperatorie și de „natura radicală” a eliminării tumorii. În prezent, se crede că rata de supraviețuire de cinci ani este de aproximativ 50%. Îmbunătățirile operaționale, în special, au făcut posibilă îmbunătățirea probabilității de supraviețuire în ultimii 25 de ani
Rata de supraviețuire scade odată cu metastazele primare. Aici rata de supraviețuire este în jur de 35%.
Șanse de recuperare
La fel ca în cazul altor tipuri de cancer, șansele de recuperare a sarcomului Ewing sunt considerate inițial ca fiind diferite în mod individual, deoarece statisticile arată doar vreodată ratele medii de recuperare și supraviețuire.
Șansele de recuperare sunt crescute dacă tumora poate fi îndepărtată complet chirurgical. Înainte de aceasta, chimioterapia trebuie făcută pentru a micsora tumora. După ce tumora a fost îndepărtată chirurgical, trebuie efectuată chimioterapie suplimentară pentru a ucide celulele tumorale rămase.
Dacă tumora nu poate fi îndepărtată complet chirurgical, șansele de recuperare sunt mult mai grave. Tratamentul de urmărire cu chimioterapie ar trebui să aibă loc și aici.
O tumoră care nu poate fi operată ar trebui iradiată cu siguranță.
În general, se poate spune că perspectiva unei vindecări a sarcomului Ewing este mai slabă dacă metastazele sunt deja prezente în momentul diagnosticării. Aceasta înseamnă că tumora s-a răspândit și crește și în altă parte a corpului.
Rata de supravietuire
Ratele de supraviețuire, în general, sunt date în medicină ca valoare statistică a „ratei de supraviețuire de 5 ani”. Aceasta indică în procente cât de mare este numărul de supraviețuitori după 5 ani într-un grup de pacienți definit. Rata de supraviețuire raportată pentru sarcomul Ewing este cuprinsă între 40% și 60-70%. Aceste zone largi rezultă din faptul că rata de supraviețuire depinde de infestarea regiunii osoase respective. De exemplu, dacă oasele brațelor și / sau picioarelor sunt afectate, rata de supraviețuire de 5 ani este de 60-70%. Dacă oasele pelvine sunt afectate, aceasta este de 40%.
Cât de mare este riscul de recidivă?
Rata de supraviețuire de 5 ani este de 50%. Aici se poate presupune că este un cancer agresiv și malign. Rata de supraviețuire de 5 ani spune că, în medie, jumătate din sarcoamele Ewing diagnosticate duc la moarte.
Cu toate acestea, dacă nu se pot detecta alte descoperiri după 5 ani de la tratamentul cu succes al sarcomului Ewing, se spune că cancerul este vindecat.
Dupa ingrijire
recomandări:
- în anul 1 și 2:
O examinare clinică trebuie efectuată la fiecare trei luni. De regulă, o verificare cu raze X locale, teste de laborator, un CT al torace și a efectuat o scintigrafie scheletică cu corp complet. Un RMN local se face de obicei o dată la șase luni. - în anul 3 până la 5:
Trebuie efectuat un examen clinic la fiecare șase luni. De regulă, o verificare cu raze X locale, teste de laborator, un CT al torace și a efectuat o scintigrafie scheletică cu corp complet. Un RMN local este de obicei efectuat o dată pe an. - Începând cu anul 6, următorul lucru se face de obicei o dată pe an
un control cu raze X cu examen de laborator și un CT al toracelui, precum și o scintigrafie scheletică a întregului corp și un RMN local.
rezumat
Boala (sarcom Ewing) și-a primit numele de la prima descriere de James Ewing în 1921. Acestea sunt tumori extrem de maligne care apar din celule neuroectodermale primitive degenerate (= celule precursoare imature ale celulelor nervoase). Astfel, sarcoamele Ewing aparțin tumorilor solide primitive, maligne și solide.
Așa cum am menționat mai sus, sarcoamele Ewing afectează în principal zonele medii ale oaselor tubulare lungi și ale pelvisului, dar este posibilă o afectare a brațului superior (= humerus) sau a coastelor, astfel încât să apară paralele cu osteosarcomul. Datorită semnelor însoțitoare de inflamație, este posibilă confuzia cu osteomielita.
Datorită metastazelor care apar foarte repede (aproximativ ¼ din toți pacienții prezintă deja așa-numitele așezări fiice în momentul diagnosticării), sarcoamele Ewing pot fi, de asemenea, găsite în țesutul moale, similar cu rabdomiosarcomele. Plămânii sunt de obicei cei mai afectați de metastaze.
Cauzele care ar putea fi responsabile pentru dezvoltarea sarcomului Ewing sunt încă necunoscute. Cu toate acestea, în prezent, se presupune că nici componenta genetică (ereditatea) și nici radioterapia care a fost deja realizată nu pot fi responsabile pentru dezvoltare. S-a constatat însă că sarcoamele Ewing apar adesea atunci când există anomalii scheletice familiale sau când pacienții suferă de retinoblastom (= tumoră malignă a retinei care apare la adolescență) de la naștere. Cercetările au arătat că celulele tumorale ale așa-numitei familii de sarcoame Ewing arată o modificare a numărului de cromozomi 22. Se presupune că această mutație (modificare genetică) este prezentă la aproximativ 95% din toți pacienții.
Sarcoamele Ewing pot provoca umflarea și durerea în regiunea / regiunile afectate, care pot fi, de asemenea, asociate cu deficiențe funcționale. Febra și leucocitoza moderată (= creșterea numărului de leucocite în sânge) sunt de asemenea concepute. Datorită posibilității de confuzie cu osteomielita, de exemplu (a se vedea mai sus), un diagnostic nu este întotdeauna ușor și, prin urmare, pe lângă procedurile imagistice (examenul cu raze X), poate fi necesară o biopsie (= examinarea țesutului unui eșantion de țesut).
Abordarea terapeutică aici este de obicei pe mai multe niveluri. Pe de o parte, așa-numitul plan de terapie prevede de obicei un tratament chimioterapeutic preoperator (= chimioterapie neoadjuvantă). Chiar și după îndepărtarea chirurgicală a sarcomului Ewing, tratamentul terapeutic de urmărire este asigurat prin radioterapie și, dacă este necesar, chimioterapie reînnoită. Aici se observă o diferență de osteosarcom: în comparație cu sarcomul Ewing, osteosarcomul are o sensibilitate mai mică la radiații.
Dacă apar sau nu recurențe (creștere reînnoită a tumorii) depinde în mare măsură de amploarea metastazelor, de răspunsul la chimioterapia preoperatorie și de „natura radicală” a eliminării tumorii. În prezent, se crede că rata de supraviețuire de cinci ani este de aproximativ 50%. Îmbunătățirile operaționale, în special, au făcut posibilă îmbunătățirea probabilității de supraviețuire în ultimii 25 de ani


.jpg)